ワンポイント15
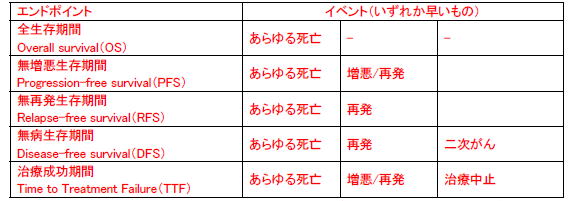
OSとPFSの違い
■OSの長所と短所
まず、エンドポイントの王様であるOSの長所と短所についてまとめる。
OSは死亡をイベントとするので、誰が評価しても明らかである。しかし、完了までに何年もかかり、数百人の患者を対象とした試験が必要となることも多い。さらに、患者が別の治療に乗り換えることにより、プロトコール治療の効果を読み取ることが難しくなる。
■PFSの長所と短所
PFSとは、患者をいずれかの群に無作為に割り付けた時点から、増悪・再発・あらゆる死亡までの期間である。増悪、再発の定義は各臨床試験のプロトコールで定義づけられる必要がある。「増悪」は、画像上のPDのほか、画像検査で確認できない原病の増悪(臨床的増悪)を指すこともある。
癌の臨床試験におけるエンドポイントとしてPFSを用いることの論議の核心は、癌の治療によって患者の生存を長らえることができない場合、"病気の進行を遅らせることに意義があるかどうか"という問題である。別の言い方をすれば、QOLと余命の長さのどちらが大事か、である。
PFSを臨床試験エンドポイントに採用する重大な利点は、腫瘍縮小効果と腫瘍安定効果の両方を検証できることである。癌細胞を殺して腫瘍を縮小させる殺細胞性の抗がん剤と異なり、今般登場している分子標的治療薬では必ずしも腫瘍縮小がみられるわけではない。このような分子標的治療薬の評価にはPFSは利点があるだろうし、最近の研究ではQOLの改善を重視する流れもあり、PFSが見直されている背景ではないか。
このほか、生存試験と比べサンプルサイズが少なくてすみ、追跡も短期間でよいという利点がある。
PFSがプライマリーエンドポイントとしてFDAが承認した薬剤の事例を挙げる。
(1)米国食品医薬品局(FDA)は一部の転移乳癌患者の治療にパクリタキセル(タキソール)と併用でベバシズマブ(アバスチン)を迅速承認した。この併用療法は、パクリタキセル単独である対照群と比較して、無増悪生存期間を5カ月改善したが、患者の全生存率(期間)(OS)の有意な改善は認めていない。
(2)FDAは最近になって、PFSの改善に基づいて、他にもいくつかの抗癌新薬、たとえば腎臓癌にソラフェニブ(ネクサバール)、卵巣癌にゲムシタビン(ジェムザール)、乳癌にイクサベピロン(イグゼンプラ)などを承認している。
しかし、生存期間のサロゲートエンドポイントとして統計的に妥当性が確認されているわけではない。評価バイアスが生じやすいこと、評価間隔をどう設定するのかが結果に影響する等の問題点が残されている。
作成日2009年4月19日